- STRONTIUM
- STRONTIUMSTRONTIUMDe Strontian, ville d’Écosse.Symbole chimique: SrNuméro atomique: 38Masse atomique: 87,62Point de fusion: 769 0CPoint d’ébullition: 1 384 0CDensité (à 20 0C): 2,54Métal alcalinoterreux mou, de reflet argenté quand il est fraîchement coupé, de couleur jaunâtre si on l’expose à l’air libre, constituant environ 0,02 p. 100 de la croûte terrestre sous forme de strontianite (carbonate) et de célestine (sulfate).Découvert en 1787 par W. Cruikshank, le strontium ne fut isolé qu’en 1808 par H. Davy par électrolyse de son chlorure mélangé à de l’oxyde mercurique sur cathode de mercure et distillation de l’amalgame formé.Finement divisé, le métal s’enflamme spontanément dans l’air. Avec l’eau, il forme l’hydroxyde de strontium avec dégagement d’hydrogène; il réagit facilement avec les halogènes, l’oxygène et le soufre. Ses sels volatils communiquent à la flamme une coloration pourpre intense, d’où son utilisation dans les feux de signalisation et les feux d’artifice.Il existe plusieurs isotopes stables et radioactifs de strontium, dont l’isotope 90 (vie moyenne de 28 ans) est un émetteur bêta abondamment produit lors des explosions nucléaires; il constitue l’élément le plus dangereux des retombées radioactives. On l’utilise dans le traitement du cancer des os. La chaleur dégagée pendant sa désintégration peut être convertie en électricité pour des piles légères de faible puissance utilisées en navigation, en météorologie et en navigation spatiale. Le titanate de strontium, SrTi3, est un matériau optique intéressant par son indice de réfraction extrêmement élevé et une dispersion optique supérieure à celle du diamant.
strontium [ strɔ̃sjɔm ] n. m.• 1829; mot angl. (1807), de Strontian, nom d'un village d'Écosse♦ Chim. Élément (Sr; no at. 38; m. at. 87,63), métal alcalinoterreux, blanc argent, mou comme le plomb. L'isotope 90 du strontium est un des plus dangereux parmi les « retombées radioactives ». Les sels de strontium sont utilisés en pyrotechnie, en médecine.
● strontium nom masculin (anglais strontium, de Strontian, nom d'un village d'Écosse) Métal alcalinoterreux, présentant de grandes analogies avec le baryum. (Élément chimique de symbole Sr.) Corps simple de numéro atomique 38, doué de propriétés comparables, du point de vue physiologique, à celles du calcium, c'est-à-dire présentant une affinité marquée pour le tissu osseux.strontiumn. m. CHIM élément alcalino-terreux (symbole Sr) de numéro atomique Z = 38.— Métal (Sr) blanc.⇒STRONTIUM, subst. masc.CHIM., MINÉR. Métal alcalino-terreux, malléable, ductile, blanc argent mais prenant rapidement une teinte jaune à l'air par oxydation, aux propriétés chimiques similaires à celles du calcium et du baryum, très disséminé dans la nature, présent dans les os et les dents, et dont il existe plusieurs isotopes stables ou radioactifs (symb. Sr, n° atomique 38, poids atomique 87,63). Méthode de datation des minéraux au rubidium-strontium; minerai de strontium. L'isotope strontium-90 fortement radioactif a été produit par les bombes thermonucléaires et représente un grand danger car il se fixe avec le calcium dans l'ossature (Sc. 1962). Les composés de strontium trouvent un usage en pyrotechnie (...), en sucrerie pour extraire le sucre des mélasses (Sr(OH)2), dans les matériaux phosphorescents (sulfure), les cathodes thermoioniques et tubes cathodiques (LESC. 1973).Prononc.:[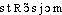 ]. MARTINET-WALTER 1973 [-
]. MARTINET-WALTER 1973 [-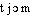 ] (7/17). Étymol. et Hist. 1816 (GAY-LUSSAC ds Ann. chim. et phys., t. 1, p. 161). Terme proposé en 1808 par le chimiste angl. Sir H. Davy [1778-1829] et formé sur strontia (v. strontiane étymol.) avec le suff. corresp. au fr. -ium (NED).strontium [stʀɔ̃sjɔm] n. m.ÉTYM. 1829, Académie, Suppl.; mot angl., nom donné par Davy (1807) au métal qu'il venait de découvrir, d'après strontianite, de Strontian. → Strontiane.❖♦ Chim. Élément (no at. 38; masse at. 87,63; symb. Sr), métal alcalino-terreux (dens. 2,6; température de fusion 771 °C), blanc argent, mou comme le plomb, ayant de nombreux isotopes, les uns stables, les autres radioactifs (certains de ces derniers ont des applications en biologie et en médecine). || L'isotope du strontium, de masse 90, est un des plus dangereux parmi les « retombées radioactives » dues aux explosions d'engins nucléaires. — Les sels de strontium colorent la flamme en rouge; certains sont utilisés en pyrotechnie, parfois en médecine.❖DÉR. Strontique.
] (7/17). Étymol. et Hist. 1816 (GAY-LUSSAC ds Ann. chim. et phys., t. 1, p. 161). Terme proposé en 1808 par le chimiste angl. Sir H. Davy [1778-1829] et formé sur strontia (v. strontiane étymol.) avec le suff. corresp. au fr. -ium (NED).strontium [stʀɔ̃sjɔm] n. m.ÉTYM. 1829, Académie, Suppl.; mot angl., nom donné par Davy (1807) au métal qu'il venait de découvrir, d'après strontianite, de Strontian. → Strontiane.❖♦ Chim. Élément (no at. 38; masse at. 87,63; symb. Sr), métal alcalino-terreux (dens. 2,6; température de fusion 771 °C), blanc argent, mou comme le plomb, ayant de nombreux isotopes, les uns stables, les autres radioactifs (certains de ces derniers ont des applications en biologie et en médecine). || L'isotope du strontium, de masse 90, est un des plus dangereux parmi les « retombées radioactives » dues aux explosions d'engins nucléaires. — Les sels de strontium colorent la flamme en rouge; certains sont utilisés en pyrotechnie, parfois en médecine.❖DÉR. Strontique.
Encyclopédie Universelle. 2012.
